Was sind eigentlich Seifenblasen?

Was sind eigentlich Seifenblasen?
Wir alle kennen die Redewendung „Der Traum zerplatzte wie eine Seifenblase!“ Ideen und Pläne erwiesen sich als nicht realistisch, sie waren vielleicht zu illusionär und ließen sich nicht erfüllen. Das jeweilige Vorhaben – obwohl verlockend – endete abrupt und glich einer Seifenblase, die leicht zerplatzen kann und dabei nichts hinterlässt. Die Seifenblase ist somit ein Symbol für Vergänglichkeit!
Seifenblasen: mehr als Spielzeug
Heute werden Seifenblasen als Bühneneffekt, in Seifenblasenshows oder als Kinderspielzeug genutzt. Aber auch Erwachsene spielen gerne mit Seifenblasen. Darüber hinaus sind Seifenblasen aufgrund ihrer Kugelform für die Naturwissenschaften und die Raumfahrt als physikalisches Phänomen interessant. Seifenblasen dienen als anschauliches Modell für mathematische Flächen, die einen minimalen Flächeninhalt haben (Minimalflächen).
Seifenblasen sind seit Jahrhunderten bekannt

Abb. 1: „Die Kinderspiele“ – Gemälde von Pieter Bruegel dem Älteren (Kunsthistorisches Museum Wien) Pieter Bruegel the Elder - Children’s Games - Google Art Project, Wikimedia Commons gemeinfrei
Als vergnüglicher Zeitvertreib sind Seifenblasen schon seit dem 16. Jahrhundert bekannt, wie das um 1560 entstandene Gemälde „Die Kinderspiele“ des flämischen Malers Pieter Bruegel des Älteren belegt (Abb. 1). Auf dem Gemälde sind 91 verschiedene Kinderspiele der damaligen Zeit dargestellt [1]. Die Erzeugung von Seifenblasen ist am unteren linken Rand des Gemäldes zu sehen (Person im hellblauen Mantel vor der braunen Mauer). Das Gemälde befindet sich im Kunsthistorischen Museum in Wien.
Zur Herstellung von Seifenblasen in Unterhaltungsshows benötigt man nicht nur künstlerisches Talent, sondern auch eine perfekte Seifenblasen-Lösung. Damit lassen sich riesige Seifenblasen erzeugen, die sogar Gegenstände und Personen einschließen können oder die mit Rauch oder Helium gefüllt sind und dann aufwärts davon schweben.
Zufallsentdeckung Pustefix®
Schon seit den 1950er Jahren spielen Kinder mit einer fertigen Seifenblasen-Lösung, die unter dem Markennamen „Pustefix®“ vertrieben wird [2] und überall gekauft werden kann. Es handelt sich dabei um eine gebrauchsfertige Lösung zur Herstellung von Seifenblasen in einer Dose mit einem roten Ring aus Kunststoff. Die Mixtur wurde 1948 durch Zufall vom Chemiker Rolf Hein beim Experimentieren und Entwickeln eines neuen Waschmittels entdeckt, wobei statt feinem Seifenschaum große schillernde Seifenblasen entstanden sind.

„Pustefix“: Alexander Klink, Pustefix Seifenblasenlauge, CC BY 3.0
Woraus bestehen Seifenblasen?
Eine Seifenblase besteht aus einem dünnen Film von Seifenwasser, der eine gewisse Menge Luft oder ein anderes Gas in einer hohlen Kugel einschließt und oft in Regenbogenfarben schillert. Wenn sich viele einzelne Seifenblasen zu einem größeren und oft bizarren Gebilde aneinanderlagern, nennt man es „Seifenschaum“.
Erstaunliche Eigenschaften im All
Dünnhäutige Gebilde, die nach kurzer Zeit leicht und spontan zerplatzen, sind Seifenblasen aber nur auf unserem Planeten. Im All haben Seifenblasen eine wesentlich höhere Stabilität (bis zu 1 Minute). Sie sind dickhäutiger und überstehen auch einen Nadelstich!
Dies bewies der deutsche ESA-Astronaut Alexander Gerst mit einem Experiment zum Verhalten von Seifenblasen in der Schwerelosigkeit im „Columbus“-Wissenschaftslabor der internationalen Raumstation ISS. Das Experiment wurde von Schülern im Rahmen des Wettbewerbs „Aktion 42“ ausgewählt, den das Deutsche Zentrum für Luft- und Raumfahrt (DLR) mit der European Space Agency (ESA) und der Stiftung „Jugend forscht“ ausrichtete [3].
Zur Chemie von Seifenblasen
Seifen nennt man die Alkalisalze langkettiger Fettsäuren [CH3-(CH2)n-COO--Me+]. Sie zählen zu den anionischen Tensiden und bestehen aus einem hydrophoben (unpolaren) Alkylrest [CH3-(CH2)n-] und einer hydrophilen (polaren) Carboxylat-Gruppe [-COO-] mit einem Na+ oder K+-Ion.
Hydrophob bedeutet „wasserabweisend“ und hydrophil „wasserliebend“. Das heißt, solche Moleküle sind an einem Ende wasserlöslich und am anderen Ende fettlöslich. Sie können damit sowohl mit polaren wie mit unpolaren Lösungsmitteln in Wechselwirkung treten. Man sagt, solche Moleküle besitzen amphiphile Eigenschaften.
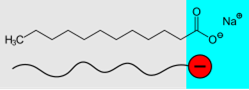
Schematischer Aufbau von Seife. (Grafik: Roland.chem, Natriumlaurinat und Tensidsymbol, CC0 1.0)
Seifenblasen bestehen nun aus einem dünnen Wasserfilm, an den sich innen und außen amphiphile Seifenmoleküle mit einer dem Wasser zugewandten polaren (negativ geladenen) Carboxylat-Gruppe und den Wasser abgewandten unpolaren Alkylgruppen anlagern. Daher entsteht eine Seifenblase immer dann, wenn sich ein dünner Wasserfilm mit Seifenmolekülen vermischt. Beim Aufblasen entsteht eine Kugelform, die aber häufig durch äußere Kräfte verzerrt ist. Von allen möglichen Formen besitzt nämlich eine Kugel die kleinste Oberfläche (Minimierung der Oberfläche) und somit die größte Stabilität.
Auf eine solche Seifenblase wirkt jedoch sofort die Schwerkraft (Erdanziehung) und der dünne Wasserfilm zwischen den beiden Tensid-Schichten wird allmählich nach unten gezogen und reichert sich im unteren Bereich der Seifenblase an. Der obere Teil der Seifenblase wird dadurch destabilisiert, Daher zerplatzen die meisten Seifenblasen in ihrem oberen Bereich [4].
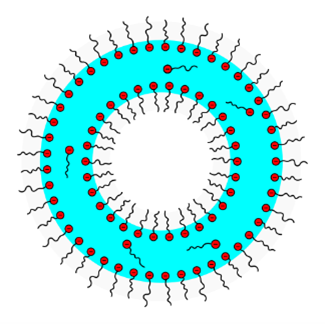
Struktur einer Seifenblase (türkisfarbener Bereich: kugelförmiger dünner Wasserfilm an den sich beidseitig die amphiphilen Seifenmoleküle anlagern – heller Bereich: eingeschlossene Luft bzw. ein anderes Gas) (Grafik: Roland.chem, Schaumbläschen, CC0 1.0)
Wichtige Rolle: Oberflächenspannung
Die Bildung einer Seifenblase ist möglich, weil auch die Oberfläche der Seifenlösung eine gewisse Oberflächenspannung besitzt und somit die Oberfläche der Seifenlösung ein elastisches Verhalten zeigt. Die Oberflächenspannung ist durch die Zugabe einer Seife aber nur etwa ein Drittel so groß wie die von reinem Wasser. „Seifenblasen“ mit reinem Wasser zu erzeugen ist extrem schwierig, weil dessen Oberflächenspannung einfach zu hoch ist und eine „Blase“ sofort zerplatzen würde. Darüber hinaus verlangsamen die angelagerten Seifenmoleküle das Verdunsten der Wasserschicht, was zusätzlich die Stabilität der Seifenblase erhöht.
In einer Flüssigkeit sind die Teilchen beweglich (thermische Bewegung) und somit wirken auf die einzelnen Moleküle sowohl abstoßende wie anziehende Kräfte. Haben die Flüssigkeitsteilchen Kontakt miteinander, so stoßen sie sich ab, während sich die Teilchen bei größeren Abständen anziehen. Im Innern einer Flüssigkeit heben sich diese Kräfte auf und die einzelnen Teilchen können sich wie Gasmoleküle frei bewegen. An der Oberfläche jedoch verbleibt eine nach innen gerichtete Kraft, die dazu führt, dass eine Flüssigkeit ihre Oberfläche so weit wie möglich zu verkleinern sucht. Will man die Oberfläche vergrößern, so muss man Energie aufwenden, um diese „Binnenkraft“ zu überwinden (Oberflächenspannung).
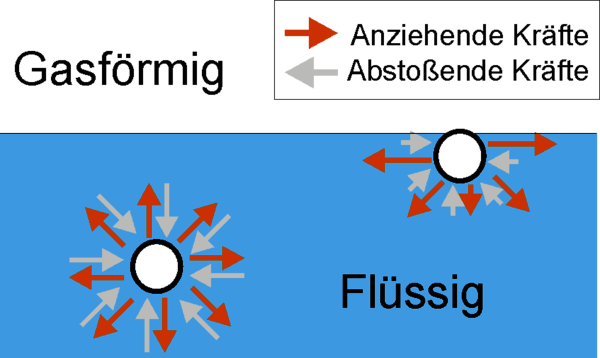
Kräfte, die auf ein Molekül in einer Flüssigkeit wirken (stark vereinfachte Betrachtungsweise) (Grafik: Galaktico, Fest fluessig grenze, CC BY-SA 3.0)
Die Oberflächenspannung ist auch Ursache dafür, dass leichte Insekten wie der Wasserläufer auf einer Wasseroberfläche laufen können oder dass nicht-benetzte Objekte, z. B. eine Büroklammer, von einer Wasseroberfläche getragen werden, solange ihr Gewicht nicht ausreicht, um die Oberflächenspannung zu überwinden. Die Oberflächenspannung zeigt sich auch daran, dass Wasser Tropfen bildet.
Seifenblasen: Schillernde Schönheiten
Bleibt abschließend die Frage zu klären, warum Seifenblasen häufig in den Farben des Regenbogens schillern. Die schillernden Farben entstehen durch Interferenz von Lichtwellen an der dünnen Haut einer Seifenblase. Da die Haut einer Seifenblase eine gewisse Dicke hat, wird Licht zweimal reflektiert, jeweils an jeder Seite der Wand. Die beiden reflektierten Lichtstrahlen besitzen unterschiedliche Wellenlängen, was zu einen Gangunterschied zwischen ihnen führt. Wenn der Gangunterschied genau die Hälfte einer Wellenlänge beträgt, fallen die Wellentäler des einen Strahls mit den Wellenbergen des anderen Strahls zusammen und die entsprechende Farbe des sichtbaren Spektrums wird ausgelöscht. Beobachtet werden dann die verbleibenden Komplementärfarben.
All die physikalischen Grundlagen (Oberflächenspannung, Kugelform, Reflexion und Interferenz) sollen die Besucherinnen und Besucher diese Webseiten nicht davon abhalten, mal wieder mit Seifenblasen zu spielen.
Ihr wisst jetzt aber, dass Seifenblasen mehr sind, als nur Luft in eine auf einem Ring aufgespannte Seifenhaut zu blasen. Seifenblasen stellen ein höchst interessantes physikalisches Geschehen dar, mit dem sich die Naturwissenschaften intensiv befassen.
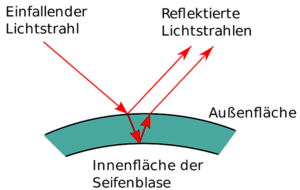
Reflexion von Lichtstrahlen an der Oberfläche einer Seifenblase
(Grafik: Reflection_from_a_bubble1.png: Saperaud derivative work: de:Benutzer:Curtis Newton, Reflexion an einer Seifenblase, CC BY-SA 3.0)
Der Beitrag wurde vom Arbeitskreis Öffentlichkeitsarbeit der Seniorexperten Chemie, einer Fachgruppe der Gesellschaft Deutscher Chemiker, erstellt.
Autor: Prof. Dr. Eberhard Ehlers (bearbeitet durch kjs, Redaktion FaszinationChemie)
Quellen
[2] de.wikipedia.org/wiki/Pustefix
[4] https://de.wikipedia.org/wiki/Seifenblase
Diesen Beitrag als pdf ausdrucken!




Kommentare
Keine Kommentare gefunden!