Strahlung, die heilen kann: Radiopharmaka

Radiopharmaka ermöglichen sowohl die präzise Diagnose von Krankheiten durch bildgebende Verfahren als auch gezielte Therapien durch selektive interne Strahlenapplikation. Bei vielen Krebserkrankungen werden Radiopharmaka erfolgreich eingesetzt, denn sie können Tumore zerstören, ohne das umliegende gesunde Gewebe zu schädigen. Forscherinnen und Forscher arbeiten an der Entwicklung kombinierter Diagnose- und Therapiewirkstoffe (Theranostika) und an personalisierten Therapieansätzen der Hochpräzisionsmedizin.
Was sind Radiopharmaka?
Radiopharmaka sind Arzneimittel, die radioaktive Nuklide (Radionuklide) enthalten und für Diagnose oder Therapie eingesetzt werden.
Radiopharmaka ermöglichen es, Krankheiten sensitiv zu erkennen und gezielt zu behandeln, indem sie entweder Stoffwechselprozesse sichtbar machen (Diagnose) oder gezielt kranke Zellen zerstören (Therapie). Die eingesetzten Mengen an radioaktivem Material sind extrem gering, die Halbwertszeiten meist kurz. Dadurch liegt die effektive Dosis einer Untersuchung im niedrigen Millisievert-(mSv)-Bereich. Ein Millisievert (mSv) ist eine Maßeinheit für die effektive Dosis ionisierender Strahlung. Die natürliche Hintergrundstrahlung in Deutschland beträgt etwa 2,1 mSv pro Jahr.
Anwendung in Diagnostik und Therapie
Die nuklearmedizinische Diagnostik kommt vor allem im Rahmen von Krebserkrankungen zum Einsatz, deckt jedoch auch andere Anwendungsbereiche ab, etwa in Form von Knochen- oder Lungenszintigraphien sowie Schilddrüsen- oder Nierenfunktionsuntersuchungen. (Eine Untersuchung mit einem Radiopharmakon nennt man Szintigrafie, das dabei entstehende Bild Szintigramm.)
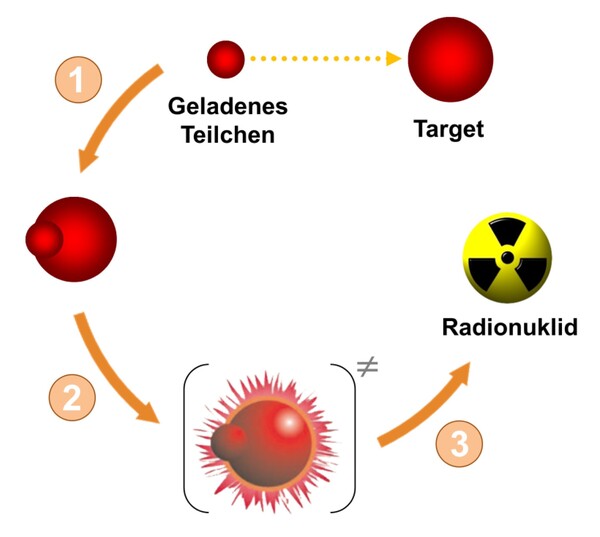
Diagnostische Radiopharmaka finden zudem breite Anwendung für die nichtinvasive Erfassung von Rezeptorsystemen oder Stoffwechselprozessen. So stellt die Gehirnbildgebung mittels PET (Positronen-Emissions-Tomographie) ein wichtiges Instrument für die Erforschung neurodegenerativer und psychiatrischer Erkrankungen dar. Bei einer PET-Untersuchung wird dem Patienten eine schwach radioaktive Substanz (Tracer) injiziert, die sich nach Bindung an ihr molekulares Target (z.B. Krebszellen mit einer erhöhten Expression des Targets) dort anreichern. Dann wird die vom Tracer ausgesandte Strahlung gemessen, wodurch wie im Fall von tumorsuchenden Diagnostika die Lokalisation des Tumors bestimmt werden kann.
Die therapeutische Anwendung von Radiopharmaka beschränkt sich bisher auf die Behandlung von Krebserkrankungen. Sie kommt vor allem bei fortgeschrittenen Prostatakarzinomen (z.B. Pluvicto® von Novartis und Xofigo® von Bayer) und neuroendokrinen Tumoren (z.B. Lutathera® von Novartis) zum Einsatz. Diese zugelassenen Radiopharmaka sind jeweils mit dem Beta-Strahler Lutetium-177 ausgestattet.
Abb. 1 zeigt das Periodensystem (Antonsusi, Periodensystem Einfach, Wikimedia Commons, gemeinfrei). Alle unterstrichenen Elemente sind radioaktiv. Für Strahlentherapie oder -diagnostik werden meist Isotopen folgender Elementen genutzt: Lutetium (71), Fluor (9), Technetium (43), Iod (53), Yttrium (39), Radium (88) oder Actinium (89).
Aktuelle Forschung und Anwendung
Der Markt für Radiopharmaka wächst sehr schnell und durch den Ausbau internationaler Kooperationen und gezielte Förderprogramme kann die Entwicklung und Zulassung weiterer diagnostischer und therapeutischer Radiopharmaka beschleunigt und vorangetrieben werden. Neben der Diagnostik und Therapie von Krebs rücken damit zunehmend die Behandlung von neurologischen, entzündlichen und Herz-Kreislauf-Erkrankungen in den Fokus der radiopharmazeutischen Forschung.
Bei diagnostischen Verfahren wie PET (Positronen-Emissions-Tomographie) und SPECT (Einzelphotonen-Emissionscomputertomographie) werden Positronen-emittierende Radionuklide wie Fluor-18 oder Gammastrahler wie Technetium-99m eingesetzt, deren Strahlung von außen mit Kameras erfasst werden kann.
Therapeutische Radiopharmaka basieren meist auf Beta-Strahlern wie Iod-131, Yttrium-90 oder Lutetium-177 bzw. Alpha-Strahlern wie Radium-223 oder Actinium-225. Da deren Zerfall gezielt zellschädigend wirkt, ermöglichen sie eine „Strahlentherapie von innen“, bei der etwa Krebszellen zerstört oder zumindest stark beeinträchtigt werden.
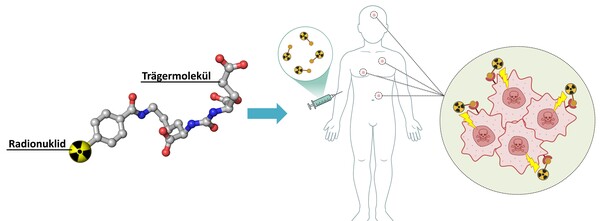
Radionuklide wie Iod-131 oder Radium-223 konzentrieren sich aufgrund ihrer biologisch-chemischen Eigenschaften direkt in den Zielorganen (Schilddrüse bzw. Knochen). Wenn kein natürlicher Anreicherungseffekt der Radionuklide besteht, werden sie durch den Einsatz radiochemischer Markierungsverfahren an ein Trägermolekül gekoppelt, das sich bevorzugt in einem bestimmten Organ oder krankhaften Zellen anreichert (Abb. 2).
Nach der Verabreichung reichert sich das radioaktive Arzneimittel in der Zielstruktur an und kann entweder pathologische Prozesse nichtinvasiv sichtbar machen oder onkologische Erkrankungen therapieren.
Sind Radiopharmaka gefährlich?
Radiopharmaka sind „radioaktive Arzneimittel“. Viele Menschen verbinden Radioaktivität automatisch mit Gefahren, ohne zwischen hochdosierten Strahlenquellen und den geringen Radioaktivitätsmengen mit zumeist kurzen Halbwertszeiten in der Medizin zu unterscheiden. Die durchschnittliche effektive Dosis einer nuklearmedizinischen Untersuchung beträgt nur etwa 5-10 mSv und entspricht somit dem zwei- bis vierfachen der natürlichen jährlichen Hintergrundstrahlung.
Nach diagnostischen Untersuchungen wird das Radionuklid meist rasch über die Nieren eliminiert. Patienten sollten daher viel trinken und für kurze Zeit den engen Kontakt zu Schwangeren und Kleinkindern vermeiden.
Die meisten medizinisch genutzten Radionuklide haben kurze physikalische Halbwertszeiten, die bei diagnostischen Radionukliden typischerweise im Bereich von Stunden und bei therapeutischen Radionukliden im Bereich von Tagen liegen. Dadurch nimmt die Strahlung nach der Verabreichung rasch ab, und die Zerfallsprodukte sind meist stabile (nicht radioaktive) Atome.
Die verabreichten Mengen sind zudem extrem gering; bei einer Behandlung mit Radium-223 erhält eine 80 kg schwere Person nur rund 2,3 Nanogramm des Radionuklids (1 Nanogramm entspricht 0,000000001 Gramm).
Strahlenschutzmaßnahmen sorgen dafür, dass Personal und Umwelt vor unnötiger Strahlenbelastung geschützt sind. Eine Deklarationspflicht für Radionuklide erleichtert die fachgerechte Entsorgung von Reststoffen.
Anspruchsvoll: Produktion und Logistik von Radionukliden
Weil die enthaltenen Radionuklide schnell zerfallen, lassen sich Radiopharmaka nicht „auf Vorrat“ herstellen und Kliniken können lediglich die nicht-radioaktiven Komponenten lagern. Die Radionuklide werden meist unmittelbar vor der Anwendung produziert, wofür komplexe Anlagen wie Teilchenbeschleuniger (sogenannte Zyklotrone) erforderlich sind (Abb. 3a-c).
Die Bereitstellung von Radiopharmaka erfolgt daher häufig über sogenannte Satellitenkonzepte, bei denen einige wenige zentrale Einrichtungen die Radiopharmaka herstellen und anschließend an Kliniken in ganz Deutschland liefern.
Der Ausbau und die Modernisierung von geeigneten Infrastrukturen, wie etwa an den Helmholtz-Zentren Dresden-Rossendorf und Jülich, ermöglichen die regionale Produktion der benötigten Radionuklide.
Wie bereits beschrieben, enthalten Radiopharmaka fast immer kurzlebige Radionuklide. Daher ist ihre Herstellung logistisch anspruchsvoll. Sie können nicht gelagert werden und müssen just-in-time produziert werden. Dafür benötigt man teure Teilchenbeschleuniger, geschultes Fachpersonal und geeignete Lieferstrukturen und Logistik. Viele Radionuklide können zudem nur mit speziellen Teilchenbeschleunigern oder Forschungsreaktoren hergestellt werden, die in Europa nicht flächendeckend zur Verfügung stehen. Bei Engpässen kann es daher zu Untersuchungsverzögerungen kommen.
Sorgfältiger Umgang mit Abfällen nötig
Rückstände aus nuklearmedizinischen Anwendungen müssen als radioaktiver Abfall entsorgt werden. Eine Entsorgung als konventioneller Abfall ist erst nach dem Abklingen möglich und erfordert eine entsprechende Freigabe. Verunreinigungen mit langlebigen Radionukliden aus dem Produktionsprozess können diese Freigabe erschweren.
Neue Radiopharmaka für personalisierte Medizin
Die Entwicklung neuer Trägermoleküle und theranostischer Paare (kombinierte Diagnose-/Therapiewirkstoffe) erhöht die Selektivität und Effektivität und ermöglicht die Einführung personalisierter Therapieansätze für die molekulare Präzisionsmedizin. Regulatorische Erleichterungen durch das Medizinforschungsgesetz beschleunigen seit Juli 2025 die Umsetzung klinischer Studien mit Radiopharmaka und stärken den Forschungsstandort Deutschland.
Obwohl Radiopharmaka neue Diagnose- und Therapieoptionen eröffnen, sind bisher nur wenige Wirkstoffe zugelassen. Klinische Studien wurden in Deutschland lange durch unterschiedliche strahlenschutz- und arzneimittelrechtliche Genehmigungsverfahren verzögert, weshalb Unternehmen oft in andere EU-Länder ausweichen. Das neue Medizinforschungsgesetz erlaubt zumindest Erleichterungen bei prospektiven klinischen Studien mit diagnostischen Radiopharmaka.

Prof. Dr. Bernd Neumaier
Institut für Neurowissenschaften und Medizin, Forschungszentrum Jülich GmbH (Foto: Uniklinik Köln)
GDCh-Fachgruppe Nuklearchemie https://www.gdch.de/netzwerk-strukturen/fachstrukturen/nuklearchemie.html
(bearbeitet durch kjs, Redaktion FaszinationChemie)
Diesen Beitrag als pdf ausdrucken!




Kommentare
Keine Kommentare gefunden!